间充质细胞治疗药物申报火热,但审评退补率居高不下。问题出在哪?
2025年12月,CDE程速远博士等人在《中国新药杂志》发表重磅综述,系统披露了MSC药物审评中的高频缺陷——从供体筛查遗漏、限传代次无依据,到STR缺失、效力检测脱节……本文提炼全文核心数据与监管红线,为研发与生产人员提供参考。

一、身份更名与国际标准更新
2025年,国际细胞治疗学会(ISCT)正式发布新标准,将沿用30余年的“间充质干细胞”更名为 “间充质基质细胞”。
综述中指出,如果企业仍希望以“干细胞”名义申报先进治疗药品,必须额外提供自我更新、多向分化等研究证明其“干性”。新标准同时明确:CD73、CD90、CD105阳性率≥95%,CD14、CD19等造血/免疫标志物阳性率≤2%,并排除了体外三向分化检测与标准贴壁生长要求,强调注明组织来源、加强效力等关键质量属性评估,终结了 30 余年细胞身份争议。
二、质量控制三大核心环节与审评常见短板
1 源头把控:供体、伦理与细胞库
1. 审评关注点:
*供体筛查:必须覆盖HIV-1/2、HBV、HCV、梅毒螺旋体;富含白细胞的供体还需检测HTLV-1/2、CMV等。需设置“最短且可靠”的检测窗口期,推荐采用监管机构批准的试剂盒。
*伦理合规:提供完整的知情同意与伦理审查文件,供体性别、年龄、病史等可追溯。
*细胞库建设:MSC库构建需要结合其多组织来源异质性及低免疫原性特性,采用主细胞库(MCB)与工作细胞库(WCB)二级体系。其中主细胞库由严格筛选的初始细胞( 如骨髓、脐带或脂肪来源原代 MSC) 扩增建立,需要全面检测细胞鉴别、活力、纯度、微生物污染及遗传稳定性等指标。
限传代次需有功能与稳定性数据支持:主细胞库传代通常不超过3~5代(P3 ~P5),工作细胞库由其传代不超过 5 代。不同来源差异明确——脐带或胎盘来源MSC在P5代内可维持高效活性;脂肪来源MSC至P8代后衰老加速(增殖下降、β-半乳糖苷酶阳性细胞增多),不建议用于系统性治疗。
*iMSC额外要求:iPSC需检测多能性(Oct4等标志物阳性率≥95%),并经免疫缺陷小鼠畸胎瘤实验验证。iMSC纯度需≥95%,遗传稳定性监测除常规核型分析外,须加做全基因组测序与全外显子测序,要求变异频率低于阈值。未分化iPSC及异常细胞残留量需验证。
2.审评常见问题:
(1)供体筛查项目不全,未考虑窗口期风险,信息追溯缺失。
(2)细胞库纯度缺乏流式验证,工作细胞库与主细胞库质量差异大时未分析操作偏差。
(3)限传代次仅凭经验,缺乏该细胞系传代稳定性与功能保留性验证数据。
(4)iMSC遗传稳定性仅做核型分析,未做测序,难排除致瘤风险。
(5)iPSC多能性验证仅靠标志物表达,未做畸胎瘤实验或无三胚层结构。
(6)iPSC残留检测未验证最低检测限,非预期细胞无特异性检测法。
2 过程管控:工艺与中间控制
1. 审评关注点:
*培养工艺:从传统二维培养转向无血清、成分明确的培养基及三维培养系统(微载体、生物反应器),是提升产量和一致性的趋势。含血清培养基成分复杂、批次差异大,可能引入病原体和异种蛋白。
*关键参数:温度、pH、溶氧等需严格监控并多批次验证。iMSC重编程阶段需使用成分精准调控的特定培养基,促体细胞向 iPSC高效转变,避免增殖或分化异常。iPSC向iMSC分化阶段,须按分化路径优化培养基。全程监测细胞群组成、纯度、标志物表达等关键指标。
*过程控制:贯彻“质量源于设计”(QbD)理念,建立完善的过程分析技术(PAT)体系。中间控制点(IPC)包括:分离后检测活率、纯度及初始表型;传代监测表面标志物与核型稳定性;收获前验证活力、无菌及功能活性。IPC结果超范围应立即停产分析。
*收获、冻存、制剂:贴壁细胞常用胰酶消化,优化离心转速与时间;制剂冻存需开展冻存及复苏工艺验证;制剂应结合剂型(如注射液、冻干粉)和给药途径(如静脉、局部注射) 优化配方与工艺,确保匹配临床需求。iMSC收获须确保细胞活力≥95%,冻存后检测关键基因表达变化。
2.审评常见问题:
(1)含血清培养基风险高,未明确内毒素等筛选指标及批次影响,缺乏伦理说明,增加病原体风险。
(2)关键参数(温度、pH、溶氧)无动态记录及预案,未按密度调整溶氧。
(3)工艺参数验证仅单次确认,未检测3批验证重复性。
(4)重编程不规范:表观遗传调控试剂(如丙戊酸)浓度数据不足,未明确时序与效率,未去除异常细胞。
(5)监测体系不完善:无分阶段监控,中期未检测部分重编程细胞。
(6)收获方法替代缺乏依据,离心参数未多批验证,洗涤后培养基成分残留。
(7)冻存程序降温参数不明,复苏后仅检测活力,未验证功能性指标。
(8)制剂未按剂型、给药途径优化配方,内包材相容性研究缺失。
(9)PAT体系不系统:仅监控温度、pH,缺少换液频率、消化时长等工艺参数记录。
(10)IPC设置不合理,结果超限无实操流程,偏差后缺乏有效分析。
3 标准制定:质量研究与放行标准
1.审评关注点:
*细胞鉴别:多维度验证。严控形态异常比例;表面标志物(CD73/CD90/CD105≥95%,CD14/CD19≤2%);分化潜能(成脂油红O染色、成骨茜素红染色、成软骨阿尔新蓝染色);STR/DNA指纹图谱(确保生产用细胞与原始细胞库遗传一致,排除交叉污染);染色体核型分析至少20个分裂相,传代多的细胞加做FISH。
*活率与增殖:活细胞数及活率(台盼蓝拒染法、CCK-8法);细胞周期(G0/G1期、S期比例);群体倍增时间(PDT)通过生长曲线监测,批间一致;PDT显著延长时结合β-半乳糖苷酶染色评估衰老;端粒酶活性优选q-PCR-TRAP法。
*微生物与安全:细菌、真菌、支原体外,外源病毒检测须覆盖HTLV-1/2、HIV等,结合供体特性(胎盘来源查人细小病毒B19)。检测方法采用“细胞培养法+PCR+新一代高通量测序(NGS)”筛查已知与未知病毒,须验证低丰度检出能力。致瘤性评估通过体外软琼脂实验和体内小鼠接种实验,iMSC需延长观察周期。
*生物学效力:须紧密关联临床作用机制。免疫调节类产品采用 “漏斗式+阶梯式”评估:先检测上清中IL-10、TGF-β等抑制因子分泌量;再经体外共培养检测对CD4+T细胞增殖的抑制率;最后在类器官或动物模型中验证炎症缓解效果,确保体外效力与体内疗效关联。组织修复类监测软骨厚度、Ⅱ型胶原蛋白表达、VEGF分泌等;归巢能力通过Transwell实验测SDF-1α趋化率或动物模型荧光标记观察24h内靶器官迁移效率。
*纯度与杂质:细胞纯度上,流式细胞术严控CD45+残余血细胞与CD90+CD105-成纤维细胞污染。工艺相关杂质(重组胰酶、牛血清白蛋白等)设定残留限值;<10μm微载体碎片靠显微计数管控。产品相关杂质须控制死亡细胞比例、<5μm细胞碎片及宿主细胞DNA残留(须控制片段长度),规避炎症与遗传风险。
*放行标准:原液须检测STR分型、核型分析、活率、数量、细胞周期、群体倍增时间、纯度、微生物、内毒素、致瘤性、生物学效力、外源因子、杂质等全项目。制剂须检测细胞鉴别、活率、数量、无菌、内毒素、支原体、渗透压、pH值、生物学效力、辅料残留等。
*iMSC额外质控:重编程因子(Oct4、Sox2等)残留用数字PCR等高灵敏度方法严控含量;强化遗传稳定性(核型+全基因组测序+甲基化分析,控制变异系数);升级致瘤性评估(体外增测细胞增殖潜能,体内延长免疫缺陷小鼠观察时间);全面验证功能等效性(与天然MSC头对头比较免疫调节、归巢、分化能力);单独验证重编程方法安全性(检测病毒载体残留与整合风险)。
2.审评常见问题:
(1)检出与重复性差:比对少、低丰度检出弱、功能学重复性差、批间变异超标。
(2)细胞鉴别仅测表面标志物,缺少STR分型防污染,核型分析分裂象不足。
(3)微生物快速检验验证仅1~2批,未覆盖多污染场景;支原体PCR检测缺少培养法复核。
(4)生物学效力:体外指标与体内疗效无对应,未覆盖细胞比例活性差异,未按适应症优化检测。
(5)杂质控制:工艺杂质限值无依据,宿主细胞DNA未控制片段长度,未评估死细胞及碎片安全性。
(6)质量标准:鉴别标准单一、无动态阈值,内毒素限值未依规设定,纯度未考虑组织来源差异。
(7)iMSC特有风险:未验证与天然MSC功能一致性,病毒载体残留及整合风险未测,分化标志物质控体系缺失。
(8)放行检测:原液缺少PDT与细胞周期检测,制剂缺少渗透压等指标,未测重组胰酶、重编程载体碎片等杂质。
三、友康GMP级间充质干细胞无血清培养基2.0:用数据直面审评痛点

1 完全无血清体系,扫除源头风险
无人源无动物源,所有蛋白人工重组,已获FDA DMF备案(31623),直接回应“含血清培养基风险高”的审评关切。
2 细胞鉴别与效力检测,覆盖“多维度”要求
综述要求细胞鉴别须结合形态、表面标志物、分化潜能;效力须与免疫调节机制关联。友康培养基培养的MSC已完成:
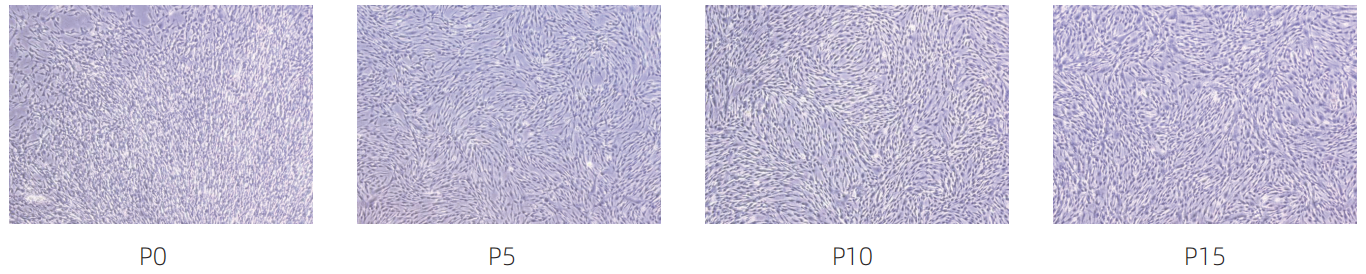
细胞形态
表面标志物
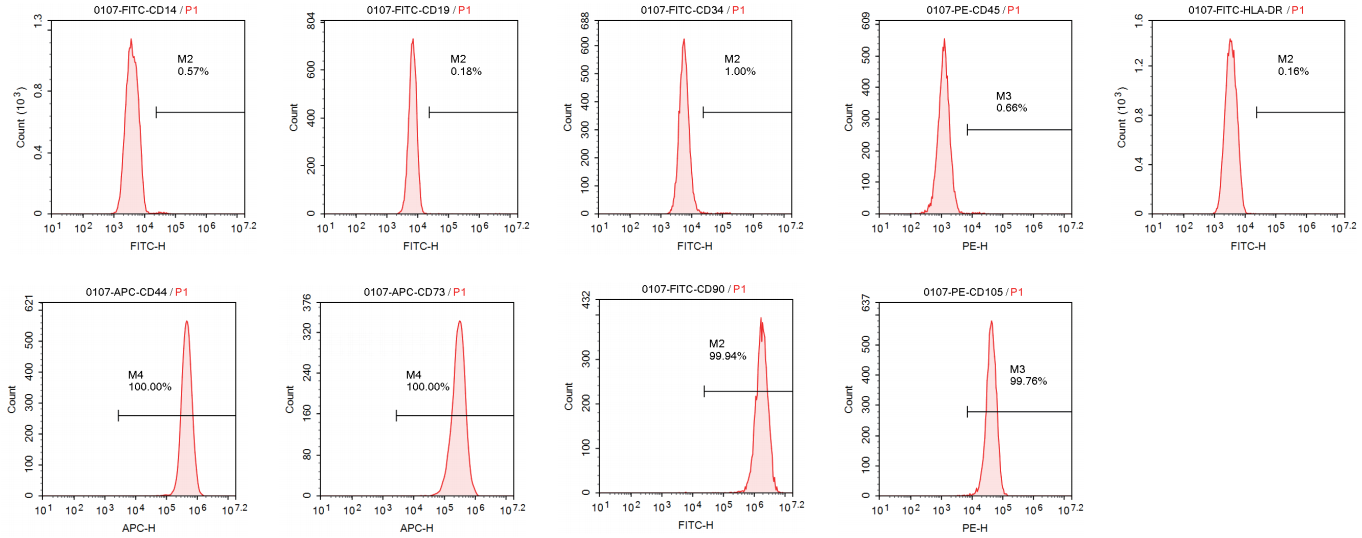
三系分化
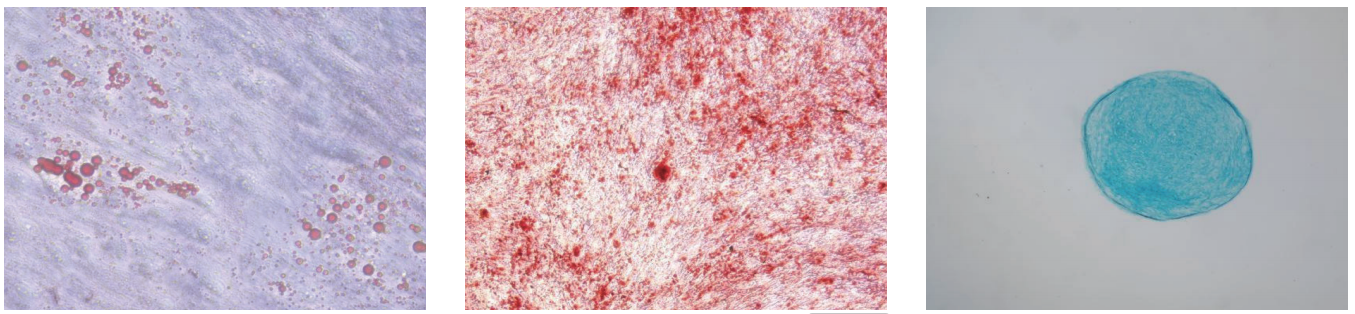 免疫调控能力
免疫调控能力
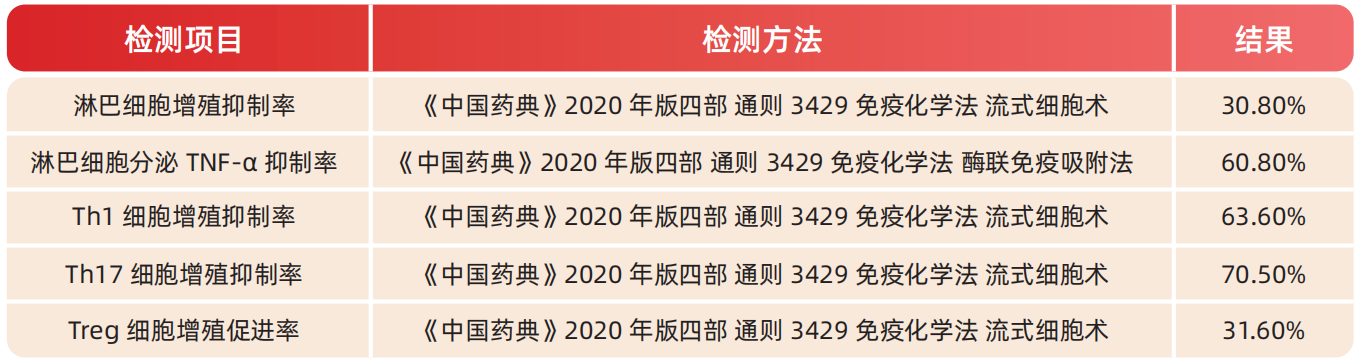
3 传代稳定性数据,支撑“限传代次”设定
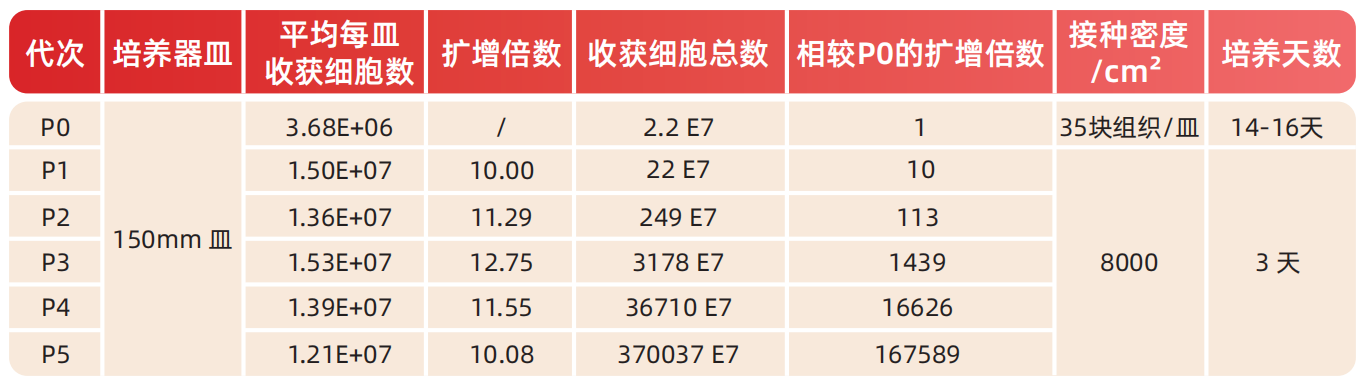
P0~P5扩增倍数稳定在10.0~12.75倍,P3代最高(12.75倍),与综述所述“早期代次功能最优”吻合。
支持传代至P20无细胞老化,为生产窗口延长提供依据,有效解决“限传代次依据不足”问题。
4 遗传稳定性与致瘤性,回应安全核心顾虑
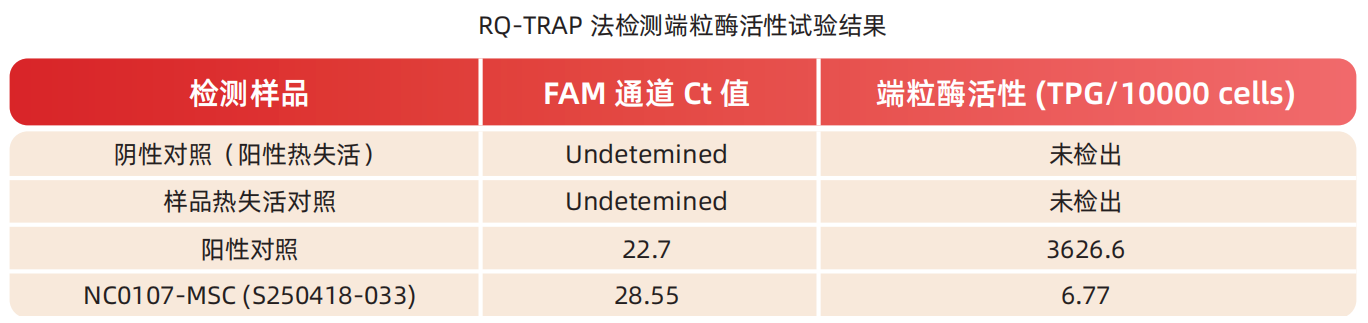
端粒酶活性:6.77TPG(正常低水平,阳性对照3626.6)。
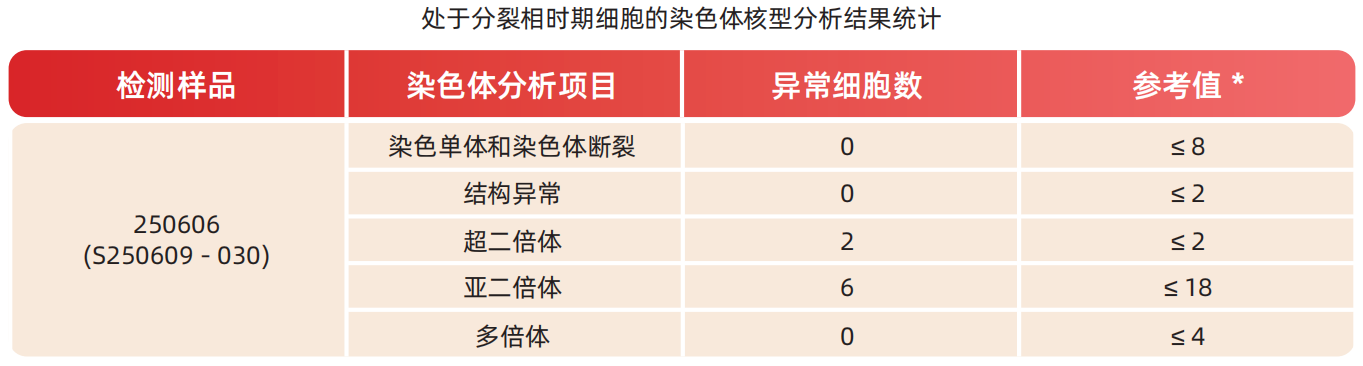
核型分析:G显带46,XX;分析100个分裂相,异常数均在药典参考值内(远超综述要求的20个分裂相)。
软琼脂克隆形成实验:无克隆形成(Hela阳性对照组大量克隆)。
5 支持iMSC培养,满足新一代产品质控要求
已验证适用于iMSC扩增与功能维持,无血清体系降低重编程因子残留干扰。
YOCON
CDE综述反复强调一个核心观点:间充质细胞治疗药物的质量可控性,是其临床转化的生命线。 从供体筛查到限传代次,从表面标志物到致瘤性评估,每一项审评要求背后,都是对细胞药物安全性、有效性与一致性的严苛拷问。
友康GMP级间充质干细胞无血清培养基2.0,不仅提供了一款成分明确、无动物源的高品质培养基,更提供了一整套可用于申报的质量研究数据,每一项都直接对应该审评要点。
选择友康,就是选择了一条从源头规避风险、用数据支撑申报的可靠路径。
如需产品手册、验证报告或体系更换方案,欢迎随时联系我们。
本文基于《中国新药杂志》2025年第34卷第24期《间充质细胞治疗药物质量控制及审评中常见问题分析》整理编写。

 友康生物
友康生物 2026-05-06
2026-05-06 行业热点
行业热点



